Methoden der Toxikologie
HPLC (high pressure liquid chromatography)
Bei der HPLC handelt es sich um ein leistungsfähiges Verfahren aus dem Gebiet der chromatographischen Trennmethoden bei der Stoffgemische getrennt werden, die in einer Flüssigkeit („Eluent, mobile Phase“) gelöst mit festen Partikeln („stationäre Phase“) in einer Trennsäule in Wechselwirkung gebracht werden. Wenn es zwischen dem Probenmaterial und der in der Säule enthaltenen stationären Phase (an Kieselgelpartikel mit einem Durchmesser von maximal < 10µm in der Säule gebunden) zu starken Wechselwirkungen kommt, so kann dieser Probenbestandteil nur langsam durch die Säule transportiert werden. Umgekehrt können Probenbestandteile, bei denen es nur zu geringen Wechselwirkungen kommt, schneller entlang der stationären Phase transportiert werden und somit auch schneller mittels des nach der Säule angeschlossenen Detektors registriert werden.
In der Regel werden die unterschiedlich starken Adsorptionen der Analytmoleküle an die Oberfläche der stationären Phasenpartikel ausgenutzt (Adsorptionschromatographie), um eine ausreichend gute Auftrennung der verschiedenen in der Probe enthaltenen Substanzen zu erreichen. Weitere einsetzbare Wechselwirkungsmechanismen sind die ionischen Wechselwirkungen (Ionenaustauschchromatographie), die unterschiedlichen Bindungsaffinitäten nicht-kovalenter Bindungen (Affinitätschromatographie) sowie eine Auftrennung nach der Molekülgröße (Größenausschlusschromatographie).
Prinzip der Adsorptionschromatographie:
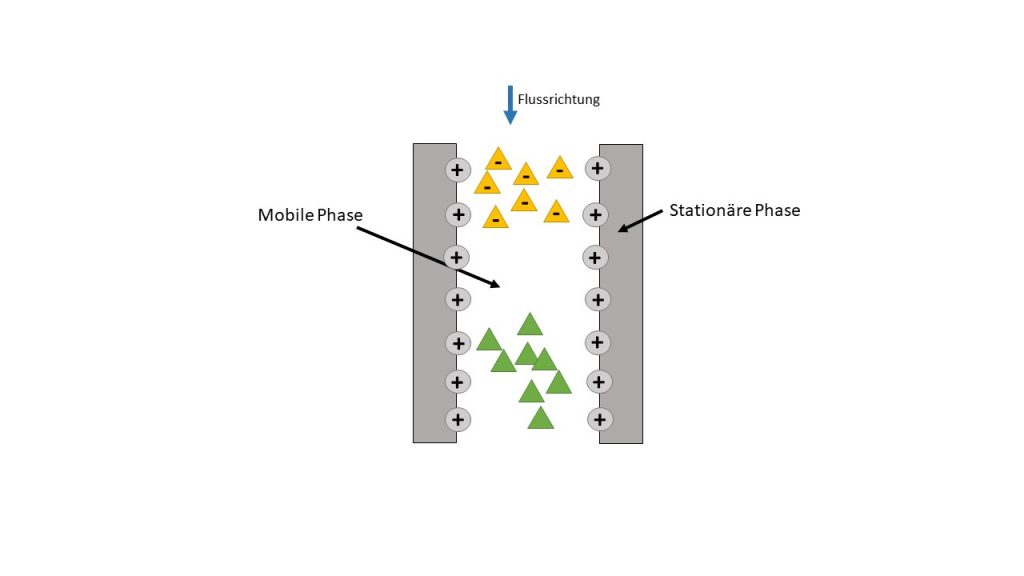
Prinzip der Ionenaustauschchromatographie:
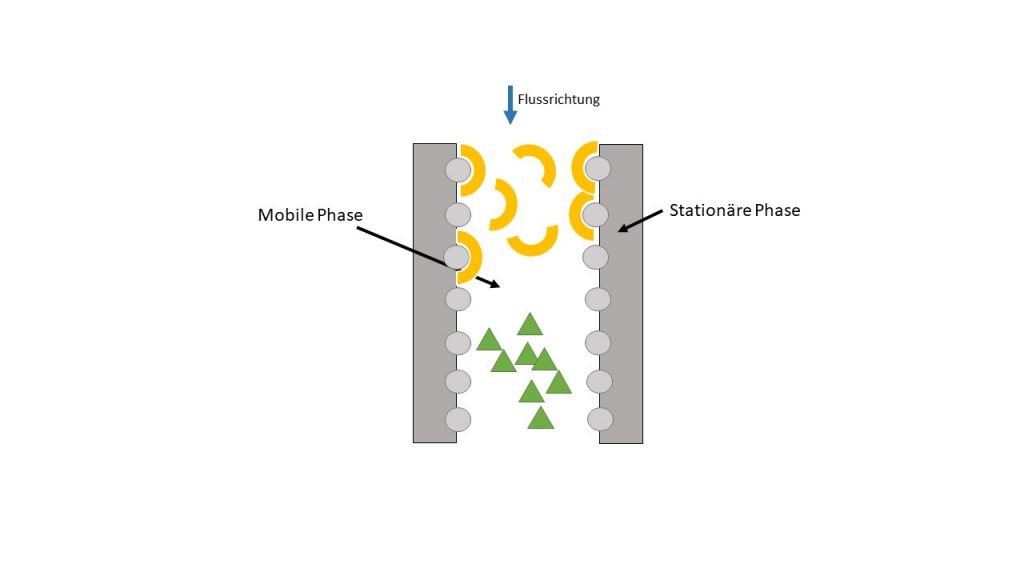
Prinzip der Affinitätschromatographie:
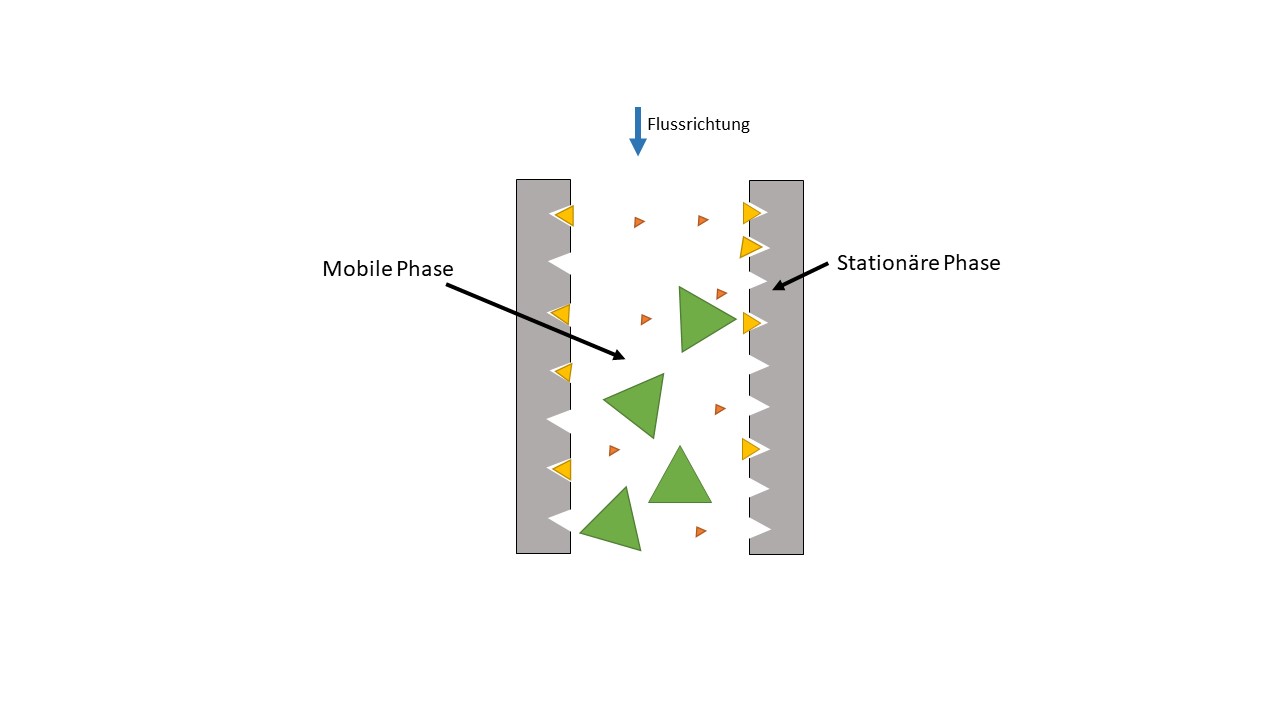
Prinzip der Größenausschlusschromatographie:
 Je geringer der Durchmesser der Partikel innerhalb der Säule ist, desto höhere Trennleistungen des HPLC-Systems können erreicht werden. Moderne HPLC-Systeme haben eine sehr gute Empfindlichkeit und können so Probenmengen im Bereich von einigen Pikogramm (1 pg = 10-12 Gramm) nachweisen.
Je geringer der Durchmesser der Partikel innerhalb der Säule ist, desto höhere Trennleistungen des HPLC-Systems können erreicht werden. Moderne HPLC-Systeme haben eine sehr gute Empfindlichkeit und können so Probenmengen im Bereich von einigen Pikogramm (1 pg = 10-12 Gramm) nachweisen.
Der allgemeine Grundaufbau eines HPLC-Systems ist stets ähnlich:
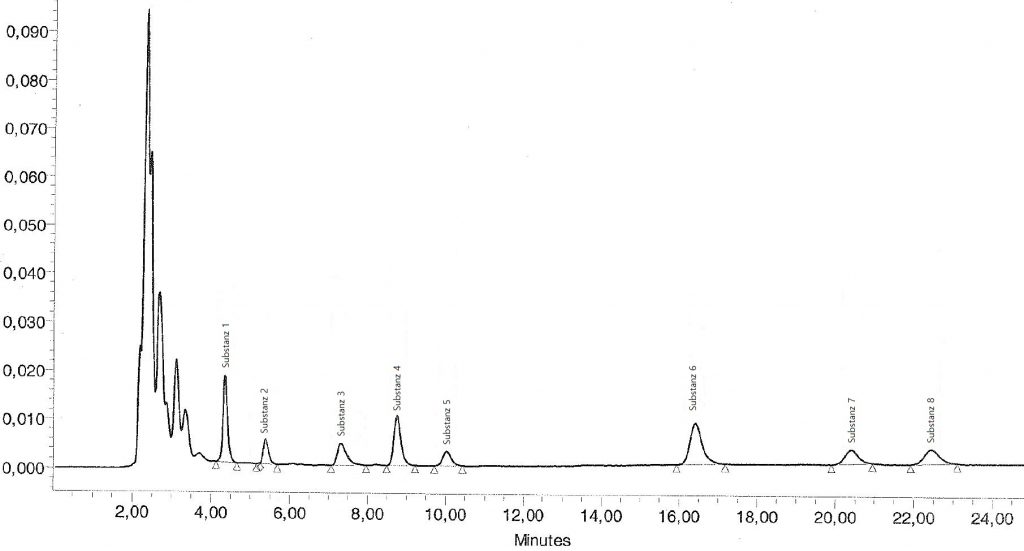
Das Fließmittel („mobile Phase“) (Abb. 1, 1) wird mittels einer Flüssigkeitspumpe (Abb. 1, 2) durch eine Kapillare mit einem sehr geringen Durchmesser an dem Probenaufgabemodul („Autosampler“) (Abb. 1, 3) und einem Heizofen (Abb. 1, 4) vorbei zur Chromatographiesäule (integriert im Heizofen, siehe Abbildung 2) gepumpt. Die Drücke innerhalb des Systems können hierbei auf bis zu 700 bar ansteigen (UHPLC). Nach dem Transport durch die Säule fließt die Probe an einem Detektor (Abb. 1, 5 und 6) vorbei und kann hier beispielsweise zu einer elektrochemischen Veränderung führen. Durch ein angeschlossenes Computersystem mit einer entsprechenden Auswertungssoftware (Abb. 1, 7) kann ein entsprechendes Chromatogramm erstellt werden. Durch die anschließende Bestimmung der AUC (area under the curve) des jeweiligen Peaks im Chromatogramm kann ein direkter Rückschluss auf die Konzentration eines Analyts innerhalb der zu untersuchenden Probe gezogen werden.


Zur Detektion nach erfolgter Auftrennung der Probenbestandteile in der Säule können je nach zu untersuchendem Analyt verschiedene Detektortypen eingesetzt werden:
UV/VIS-Detektor(HPLC-UV):
UV-Detektoren werden am häufigsten verwendet. Prinzipiell sind Festwellenlängendetektoren, variable UV-Wellenlängendetektoren oder Photodiodenarraydetektoren verfügbar. Je nach zu untersuchendem Analyt und dessen Adsorptionsmaximum wird die optimale Wellenlänge ausgewählt, um eine optimale Kombination aus Sensitivität und Spezifität der verwendeten Methode zu gewährleisten.
Fluoreszenz-Detektor (HPLC-FLD):
Wenn die zu analysierende Substanz fluoresziert, so kann mittels eines Fluoreszenzdetektors eine deutlich höhere Sensitivität als mit einer UV-Detektion erreicht werden.
Elektrochemischer Detektor (HPLC-ECD):
Einige Stoffe können sehr empfindlich mittels einer initialen elektrochemischen Redox-Reaktion und der hieraus resultierenden Änderung des Elektrodenpotenzials nachgewiesen werden. Zur kontinuierlichen Aufzeichnung des Elektrodenpotenzials werden elektrochemische Detektoren eingesetzt.